72
3
7.
LA RADIACTIVIDAD
Los núcleos de los átomos de algunos elementos no son estables, porque tienen un
número de neutrones muy superior al de protones. Para conseguir la estabilidad, estos
núcleos emiten partículas y radiaciones de forma espontánea. Cuando emiten partículas
se transforman en núcleos de átomos de otros elementos. Este fenómeno, que es
exclusivamente nuclear, recibe el nombre de
radiactividad
y fue descubierto en 1896
por
H. Becquerel,
con el uranio.
¿Qué evidencias experimentales consideras que hay de la radiactividad?
Las radiaciones emitidas por los núcleos de estos átomos tienen la capacidad de impre-
sionar placas fotográficas, ionizar gases, producir fluorescencia e, incluso, dañar los te-
jidos de los seres vivos. Estas radiaciones pueden ser de tres tipos:
alfa
,
beta
y
gamma.
❚❚
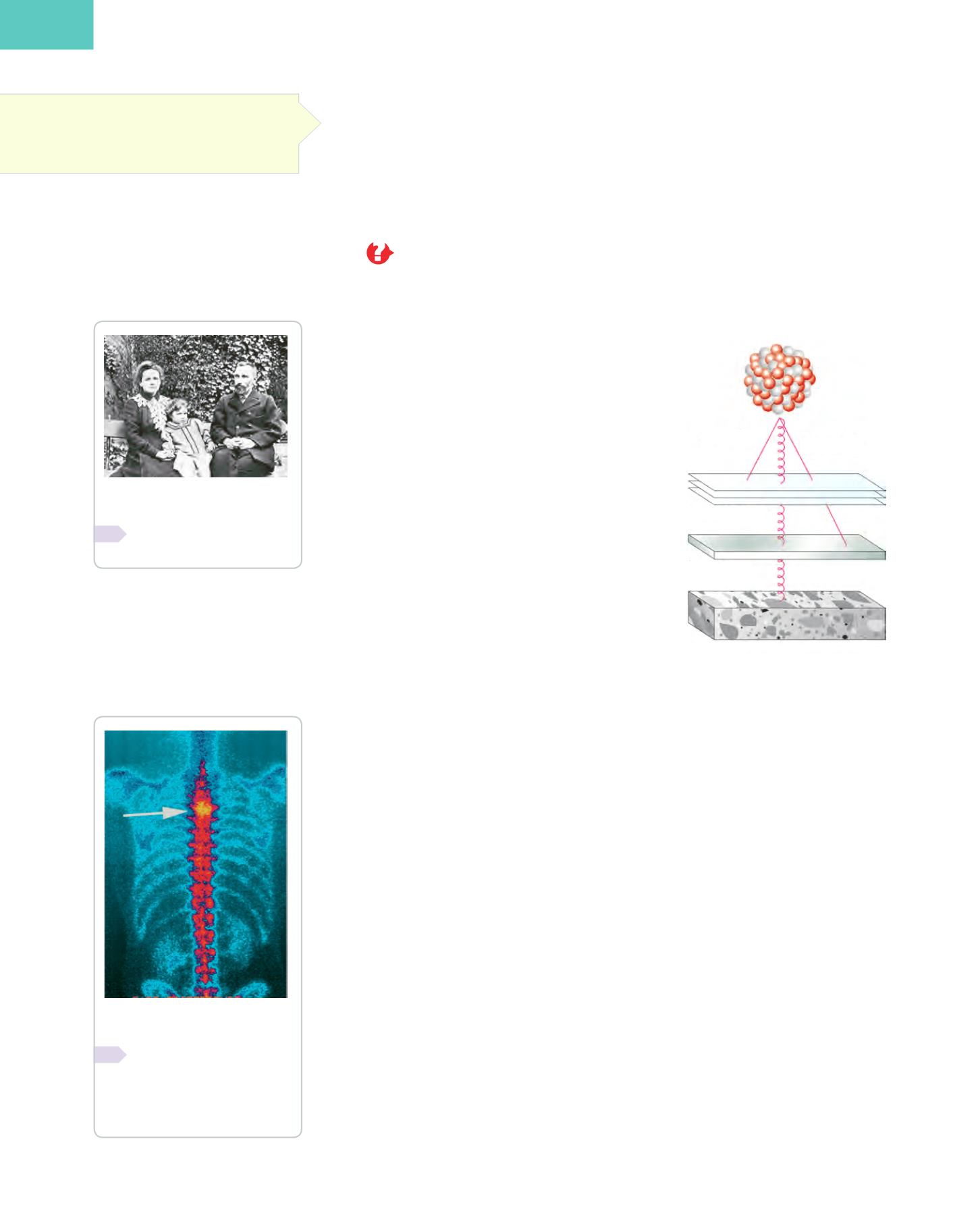
Radiación alfa,
α
.
Está formada por
partí-
culas
α
que constan de dos protones y dos
neutrones, por tanto, tienen
carga positiva.
Son emitidas por los núcleos a gran velocidad,
aunque se frenan rápidamente en el aire. Su
poder de penetración
es escaso: unas pocas
hojas de papel son suficientes para detenerlas.
❚❚
Radiación beta,
β
.
Está formada por electro-
nes, es decir, tienen
carga negativa
y se des-
plazan a gran velocidad. Poseen un
gran poder
de penetración
y son capaces de atravesar lá-
minas de aluminio de hasta 5 mm de espesor.
❚❚
Radiación gamma,
γ
.
Es una radiación de
alta energía que
no tiene carga eléctrica
y
que se propaga a la velocidad de la luz. Los
rayos gamma son capaces de atravesar finas
capas de metal y penetrar en el cuerpo de los
animales y del ser humano; sin embargo, pue-
den detenerlos las láminas de plomo u hormi-
gón de más de 25 mm de espesor.
7.1.
Los radioisótopos
Los
radioisótopos
son isótopos radiactivos de un elemento. Por ejemplo, el carbo-
no-14,
14
6
C, es un isótopo radiactivo del carbono. Otros son el
219
86
Rn, el
226
88
Ra y el
235
92
U.
Un isótopo radiactivo es, desde el punto de vista físico y químico, totalmente idéntico
a un isótopo inactivo. Sin embargo, el radioisótopo es un átomo marcado al cual po-
demos seguir en todos los procesos químicos y biológicos gracias a las radiaciones que
emite, de ahí sus múltiples aplicaciones.
7.2.
Aplicaciones de los radioisótopos
7.2.1.
Medicina
Los isótopos radiactivos se utilizan en medicina para el
diagnóstico
y el
tratamiento
de muchas enfermedades. Los que se emplean para el
diagnóstico
emiten radiaciones
que no dañan los tejidos vivos. Se suministran a los pacientes disueltos en una sustan-
cia que les permite llegar hasta el órgano que se va a investigar.
Para el
tratamiento
se utilizan dosis de isótopo mayores. La cantidad de radiación
debe ser controlada para que destruya únicamente las células dañadas y no los tejidos
sanos.
Así, en el
diagnóstico
del cáncer de tiroides se suministra
132
I, cuya radiación no causa
problemas. Sin embargo, en la
terapia
de este tipo de cáncer se utiliza
131
I, que emite
partículas que pueden destruir las células cancerosas.
❚❚
Los isótopos son átomos
de un mismo elemento que
tienen igual número atómico
pero distinto número másico.
Marie Curie, Pierre Curie y su
hija Irene.
Busca información y escri
be la biografía de Marie Curie.
29
Diagnóstico médico mediante
uso de isótopos radiactivos.
La imagen muestra una
gammagrafía ósea. Busca
información acerca de esta
prueba diagnóstica y anota
sus aplicaciones
.
30
Poder de penetración de las
diferentes radiaciones.
Partículas
α
Partículas
β
Rayos
γ
Lámina
de aluminio
Hojas de papel
Hormigón


