107
6. Las reacciones químicas
+
www
4.
¿EN QUÉ PROPORCIÓN REACCIONAN ENTRE SÍ
LAS SUSTANCIAS?
¿Pueden reaccionar las sustancias entre sí en cualquier proporción?
Nuestra hipótesis es que las sustancias no reaccionan en cualquier proporción. Para
averiguar si es correcta, recurrimos a la experimentación.
Hacemos reaccionar diferentes cantidades de azufre con diferentes cantidades de co-
bre para obtener determinadas cantidades de sulfuro de cobre. Como puedes observar,
en algunos de los experimentos se consumen todo el azufre y el cobre, pero en otros
sobra azufre o cobre.
Experimento
Masa de
azufre
Masa de
cobre
Masa de
sulfuro de
cobre
Masa de
azufre
sobrante
Masa de
cobre
sobrante
1
0,25 g
1,00 g
1,25 g
0
0
2
0,25 g
1,15 g
1,25 g
0
0,15 g
3
0,50 g
1,00 g
1,25 g
0,25 g
0
4
0,75 g
3,00 g
3,75 g
0
0
A la vista de los datos obtenidos en los experimentos el siguiente paso es analizarlos.
Para ello podemos responder a las siguientes cuestiones:
❚❚
¿Se cumple la ley de conservación de masa en los cuatro experimentos?
❚❚
Calcula la relación masa de cobre/masa de azufre en los experimentos 1 y 4.
❚❚
Indica la masa de cobre que reacciona con los 0,25 g de azufre del experi-
mento 2. ¿Sobra cobre? ¿Por qué?
❚❚
Indica la masa de azufre que reacciona con 1,00 g de cobre del experimen-
to 3. ¿Sobra azufre? ¿Por qué?
Las conclusiones obtenidas son:
1.
Las sustancias
no
reaccionan entre sí en cualquier proporción.
2.
La relación entre las masas que reaccionan es siempre
constante.
masa de cobre
masa de azufre
=
1,00
0,25
=
3,00
0,75
=
4
Experimentos como estos llevaron a
L. J. Proust
a enunciar, en 1779, la
ley de las
proporciones constantes,
también conocida como
ley de Proust:
Cuando dos o más elementos se combinan para dar un mismo compuesto, lo ha-
cen siempre en una
proporción de masas definida
y
constante.
Esta ley nos permite distinguir entre una mezcla homogénea y un compuesto.
Una
mezcla homogénea
puede estar formada por los mismos componentes que un
compuesto, pero admite diferentes proporciones, mientras que un
compuesto
tiene
siempre una sola e invariable proporción.
Indica cuáles de estos enunciados son verdaderos o falsos y escribe de forma
correcta los que sean enunciados falsos:
a)
La
relación entre las masas de cobre y las masas de azufre que reaccionan
para dar sulfuro de cobre puede ser constante e igual a 3.
b)
Una mezcla homogénea de azufre y limaduras de cobre puede estar for-
mada por una proporción de 1 a 4, 1 a 3 y 1 a 5.
c)
Cuando el sulfuro de cobre se descompone en azufre y cobre se obtiene
cobre y azufre en la proporción 4 a 1.
16
Ideas claras
❚❚
Los átomos de elementos que
se combinan para formar un
mismo compuesto siempre lo
hacen en una relación de nú-
meros enteros sencillos. Solo
existe una proporción sencilla.
❚❚
La masa total de las
sustancias que intervienen
en una reacción química se
conserva.
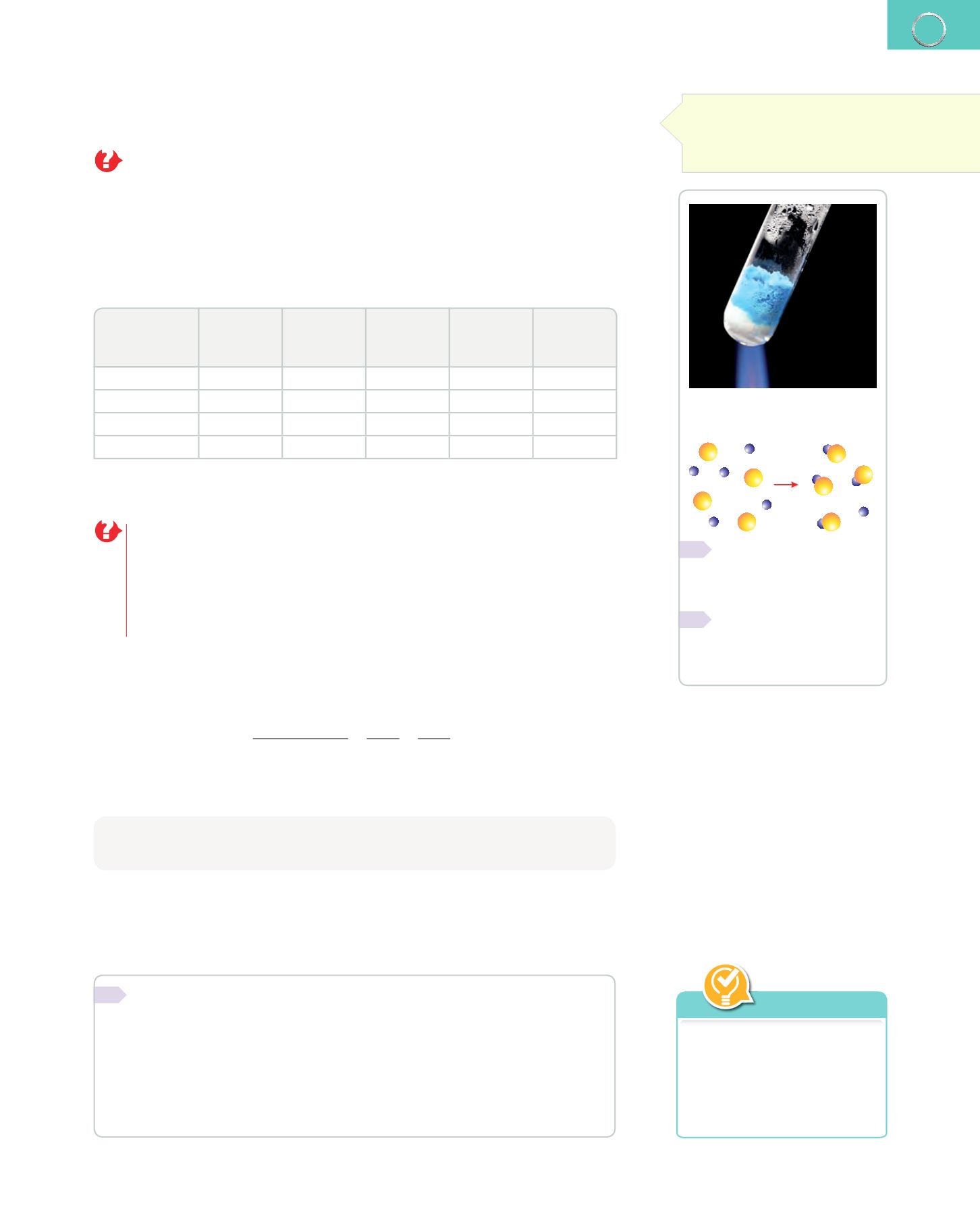
Reacción del cobre y el azufre
para dar sulfuro de cobre.
¿En qué proporción re-
accionan los átomos de azufre
y los átomos de cobre en esta
reacción química?
Dibuja los átomos de
esta reacción de manera que
no haya exceso de ningún ele-
mento.
14
15


